
Anvisa aprova registro de vacina e de medicamento contra covid-19
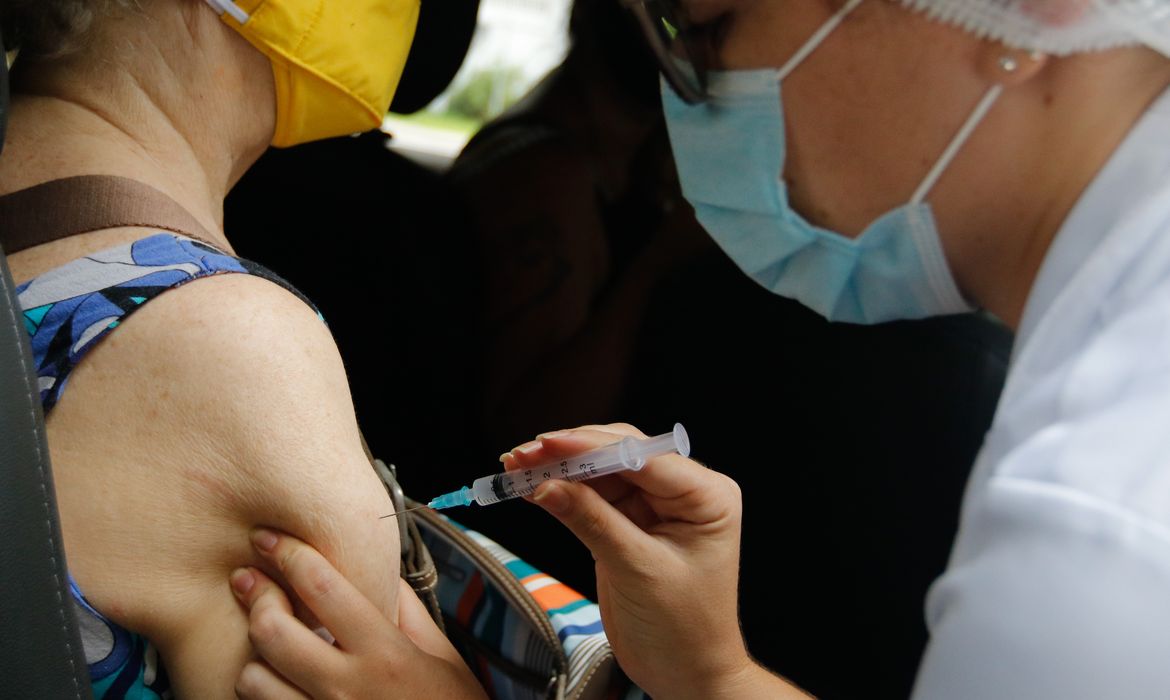 |
| Foto: Tânia Rego/Agência Brasil |
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou, nesta sexta-feira (12), a aprovação do primeiro medicamento com indicação em bula para tratamento de pacientes infectados pela covid-19, o antiviral Rendesivir.



A mesma medicação, da biofarmacêutica americana Gilead Sciences, também foi aprovada no ano passado para uso como medicamento oficial para o tratamento da covid-19 pela Food and Drug Administration (FDA), órgão norte-americano equivalente à Anvisa.
Vacina de Oxford
No anúncio, o gerente-geral de Medicamentos e Produtos Biológicos da agência, Gustavo Mendes, disse que a Anvisa também concedeu o registro definitivo à vacina da AstraZeneca/Oxford, que já tinha autorização para uso emergencial no país, assim como a CoronaVac, produzida pelo Instituto Butantan, em São Paulo.
O primeiro imunizante a obter o registro definitivo no Brasil foi o da Pfizer
Com a liberação, a vacina do consórcio AstraZeneca/Oxford terá uma etapa de produção no Brasil, na Fundação Oswaldo Cruz (Fiocruz). A autorização permite que a vacina seja aplicada em maiores de idade.
Confira o anúncio:
Desenvolvimento de vacinas
Para ser aprovada, a vacina precisa passar por estágios de desenvolvimento. O estágio inicial é feito em laboratório, com análise do vírus e de moléculas para definição da melhor composição do produto, explica a Anvisa.
Depois, a vacina é testada em animais, que são expostos ao agente causador da doença. Na etapa de estudos clínicos com três fases, são feitos testes em humanos desde que se tenha dados preliminares de segurança e possível eficácia.
Para liberar o registro do imunizante, técnicos especializados da Anvisa revisam todos os documentos para validar a segurança da vacina.
Edição: Kelly Oliveira
Por Karine Melo - Repórter da Agência Brasil - Brasília
Assinar:
Postar comentários (Atom)
Siga-nos
Total de visualizações de página
Ouça aqui: Web Radio Gospel Ipiaú
Web Rádio Gospel de Ipiaú

Mercadinho Deus te Ama

Faça seu pedido: (73) 98108-8375


Publicidade

Publicidade

Publicidade

Publicidade

Publicidade.

Publicidade

Anucie aqui: (73) 991241546-9-82007563









Nenhum comentário:
Postar um comentário
Comente esta matéria.